化妆品创新的源头在哪里?答案往往指向原料。一款全新的活性成分,可能催生一个爆款品类,甚至重塑一个细分赛道。但新原料要进入市场,必须通过国家药监局的备案或注册——这个流程有多复杂?需要准备哪些资料?2026年新政又带来了哪些变化?
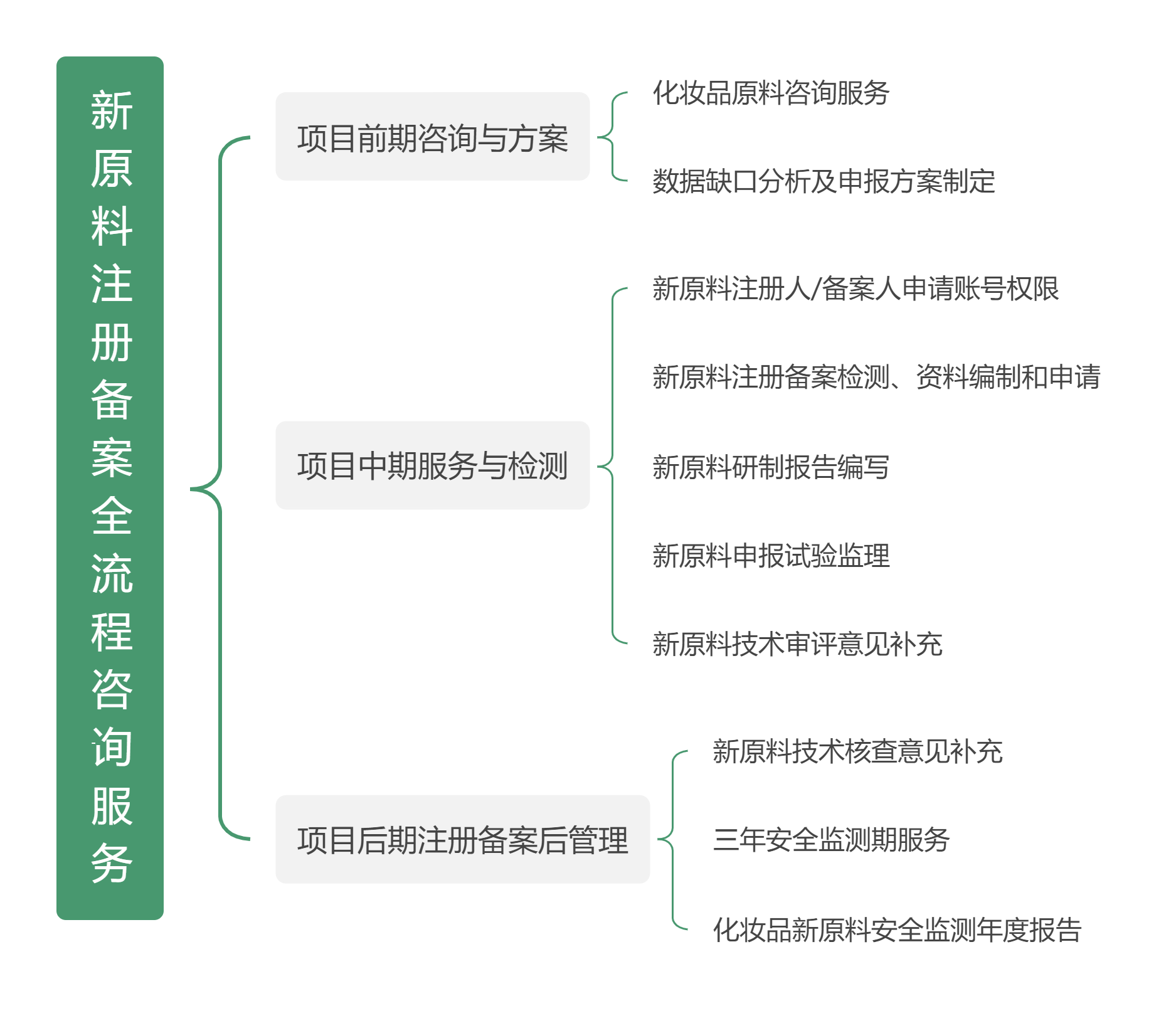
根据2026年1月国家药监局发布的《支持化妆品原料创新若干规定》,新原料实行科学分类管理,建立不同类别的评价标准和技术要求。化妆品新原料备案流程涵盖分类界定、资料准备、安全性评估、技术审评等多个环节,是原料从实验室走向市场的必经之路。
一、新原料分类界定:确定属于哪一类原料
1、判断是否属于新原料:首先确认该原料是否在《已使用化妆品原料目录》中。若不在目录中,则属于新原料,需要办理备案或注册。根据2025年发布的《支持化妆品原料创新若干规定》,新原料实行科学分类管理,根据风险程度高低建立不同类别的评价标准和技术要求。
2、确定备案还是注册:根据《化妆品监督管理条例》,具有防腐、防晒、着色、染发、祛斑美白功能的新原料,以及较高风险的新原料,需要办理注册;其他新原料办理备案即可。备案和注册的流程、资料要求和审批周期存在差异。
3、原料安全风险评估:对原料的毒理学数据、使用历史、暴露量等进行全面评估,确定原料的安全性等级和风险控制措施。
二、备案/注册资料准备
1、原料基本信息:包括原料名称(INCI名、化学名、商品名等)、CAS号、分子式、分子量、纯度、来源(化学合成、植物提取、发酵等)、生产工艺概述等。
2、安全性评估资料:这是新原料备案的核心内容。根据新规,不同风险等级的新原料需要提交不同深度的毒理学资料。对于低风险原料,可减免部分毒理学试验报告。若原料已在国外上市多年且有充分的安全性使用历史,可提交相关证明文件替代部分试验。
3、质量控制标准:包括原料的理化指标、检测方法、规格要求、储存条件、保质期等。需提供至少3批代表性样品的检验报告。
4、使用目的与使用限制:明确原料在化妆品中的使用目的(如保湿剂、抗氧化剂、表面活性剂等)、建议使用浓度、适用产品类型、禁忌事项等。
5、境外上市证明(如适用):对于已在其他国家或地区上市的新原料,可提交境外上市证明文件。根据2026年3月《关于化妆品注册备案有关事项的公告(征求意见稿)》,国际化妆品新品在中国首发上市的,免于提交在生产国已经上市销售的证明文件。
三、提交申请与技术审评
1、系统申报:通过国家药监局化妆品注册备案信息服务平台提交新原料备案/注册申请。需填写完整信息并上传所有资料电子版。
2、形式审查:监管部门对申报资料进行形式审查,确认资料是否齐全、格式是否符合要求。通过后进入技术审评环节。
3、技术审评:技术审评机构对原料的安全性、质量可控性、使用必要性等进行全面评估。审评过程中可能会要求补充资料或澄清问题。根据新规,新功效化妆品和新原料将设置专门审评通道,实施即报即审。
4、审评结论:审评通过后,备案原料获得备案编号,注册原料获得注册批件。备案原料在获得备案编号后即可用于化妆品生产;注册原料需等待批件下发后方可使用。
四、备案后管理与安全监测
1、安全监测期管理:根据《化妆品监督管理条例》,新原料备案后设有3年安全监测期。监测期内,使用该原料的化妆品需要每年提交安全性监测报告,发现安全问题的需立即采取措施。
2、年度报告提交:新原料备案人需要在每年规定时间内提交年度报告,包括原料的使用情况、安全性监测数据、国内外监管动态等。
3、信息变更与注销:若原料信息发生变化(如生产工艺变更、质量控制标准调整等),需及时办理变更备案。若原料不再使用,可申请注销备案。
4、监测期后管理:安全监测期满后,若未发现安全问题,原料将纳入《已使用化妆品原料目录》,成为已使用原料。
化妆品新原料备案是化妆品创新的“第一道门”。2026年国家药监局出台的《关于深化化妆品监管改革促进产业高质量发展的意见》明确提出,将支持化妆品原料技术创新,畅通新功效化妆品注册渠道,优化审评审批程序。对于原料企业而言,掌握新原料备案流程,提前规划安全性评价方案,是抢占创新赛道的关键。同时,使用新原料的化妆品品牌也需关注原料的备案状态和监测期要求——使用尚未完成安全监测期的新原料,需要额外提交毒理学试验报告。
汇策集团轻工检测作为专业的化妆品、日化品第三方检测机构,拥有CMA和CNAS双资质认证,实验室严格遵循ISO/IEC 17025管理体系运行。我们为新原料研发企业提供从毒理学试验、安全性评估、理化检测到备案资料咨询的全流程技术支持,帮助客户高效完成新原料备案,抢占原料创新先机。欢迎联系专业工程师获取化妆品新原料备案专属方案。
 alt="微信二维码">
alt="微信二维码">